허가심사 투명성·신뢰성 강화 위한 허가 현황 안내
식약처(처장 오유경)는 의료제품 허가심사에 대한 투명성과 신뢰성을 강화하기 위해 6월 의료제품 허가 현황을 제공했다.

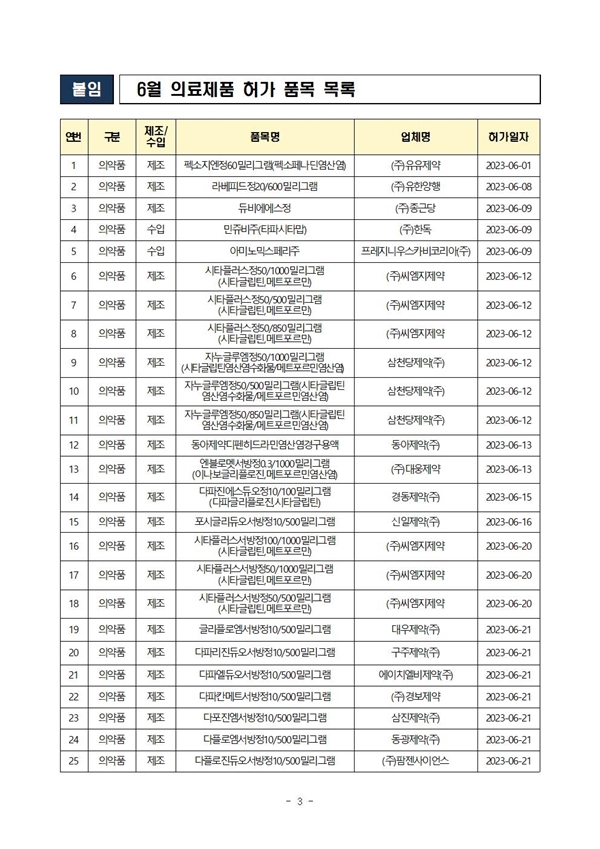
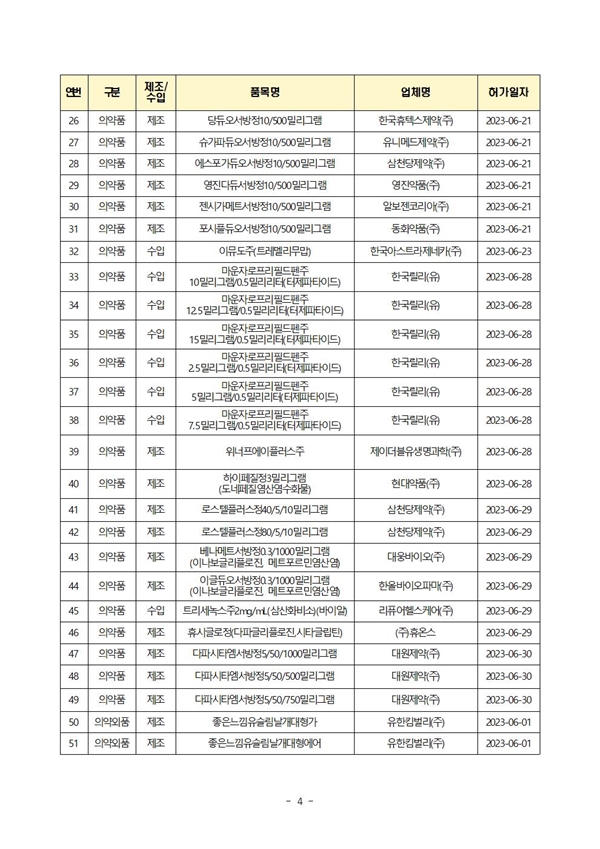
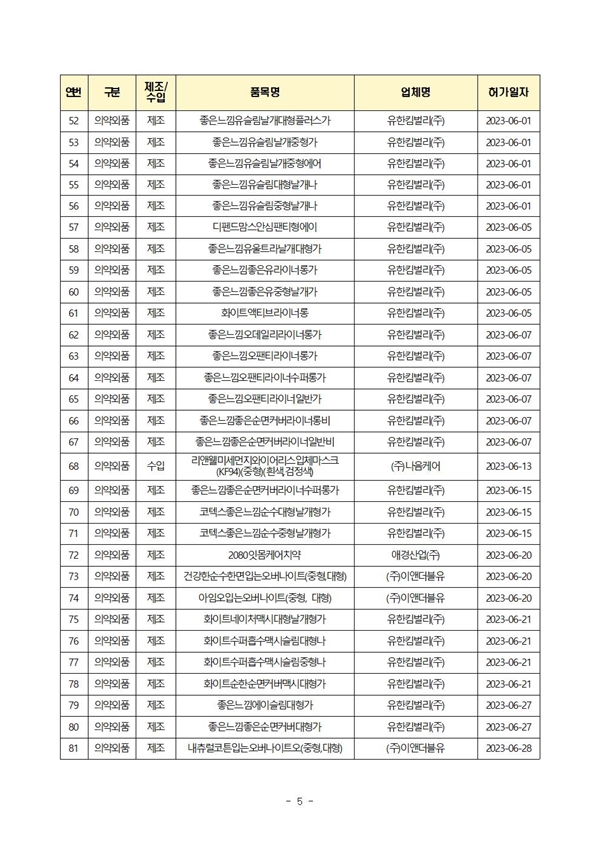
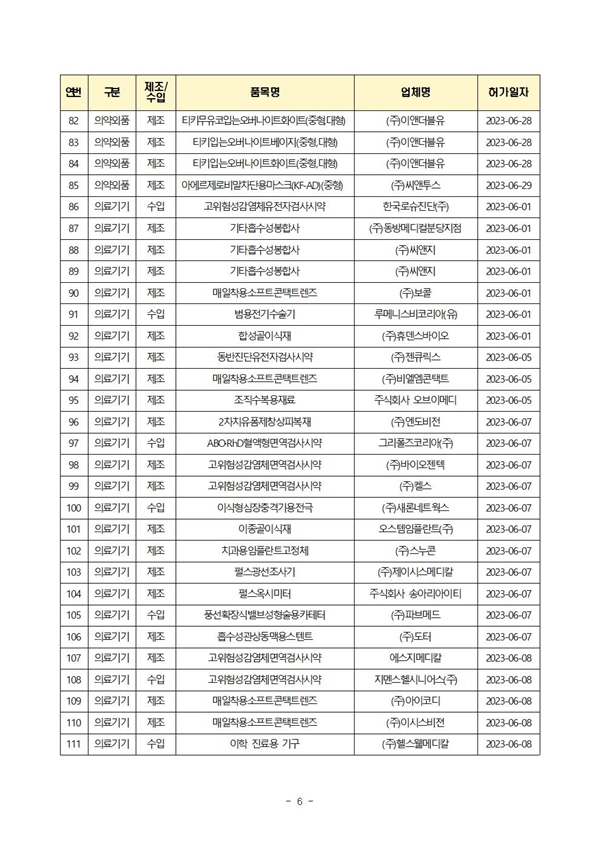
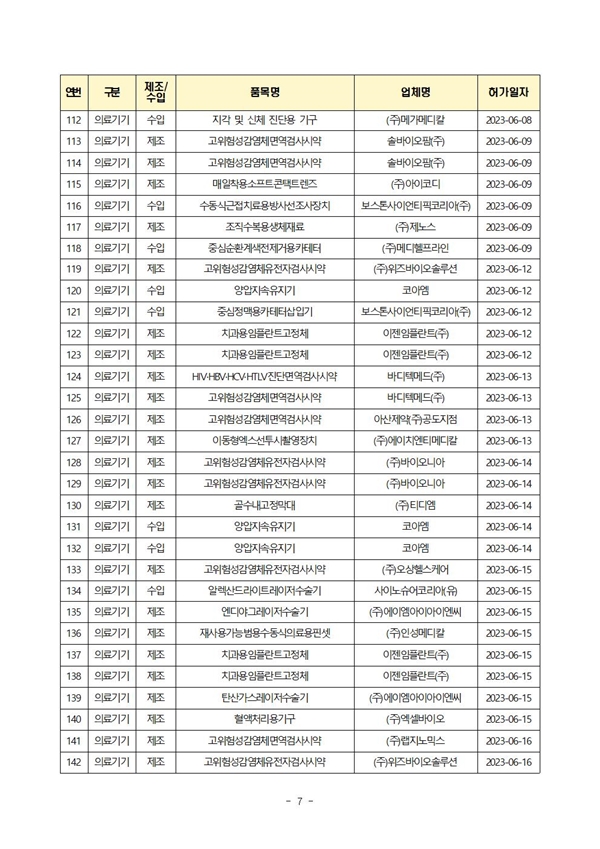
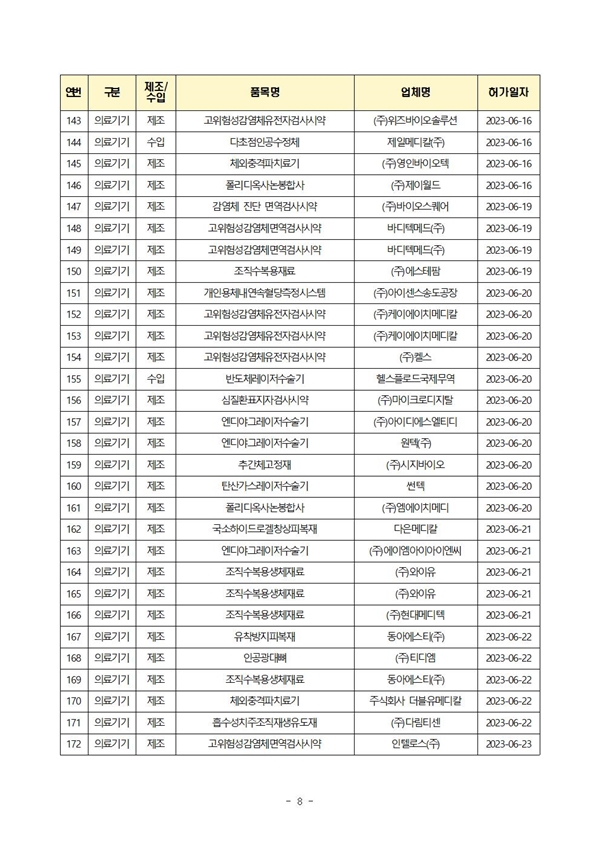
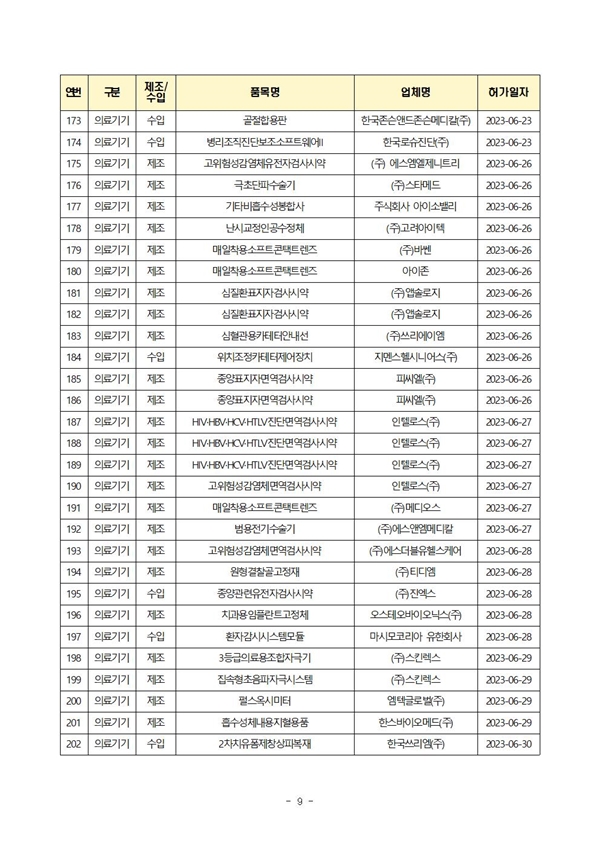
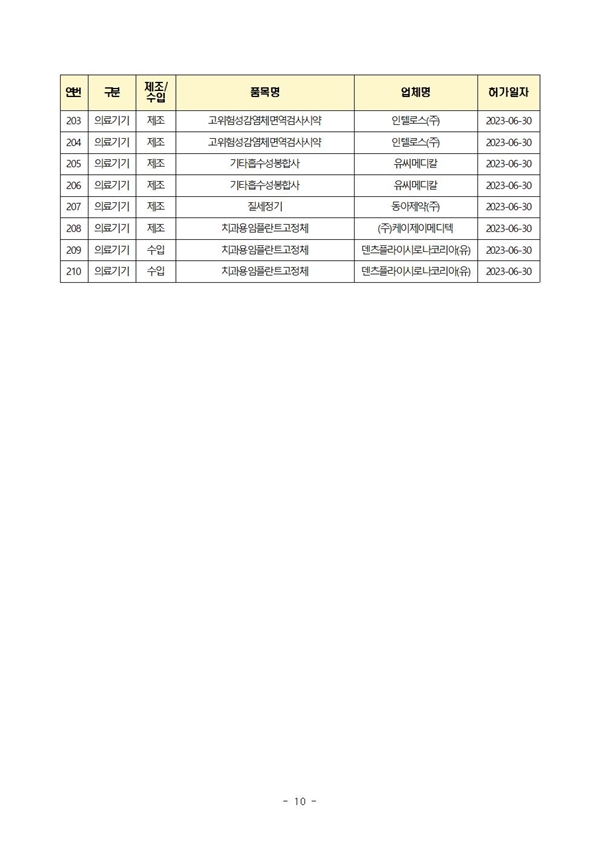
식약처(본부)는 6월에 의료제품 총 210개 품목을 허가했으며, 이 중 제조는 174개 품목, 수입은 36개 품목이었다.(2023년 누적: 총 1,078품목)
<의료제품 허가 현황>
| 구분 | 6월 (6.1. ~ 6.30.) |
올해 누적 (2023.1.1. ~ 6.30.) |
| 계 | 210 | 1,078 |
| 의약품 | 49 | 408 |
| 의약외품 | 36 | 79 |
| 의료기기 | 125 | 591 |
| 의료제품별 허가 현황 안내 대상 (의약품) 신약, 자료제출의약품, 특수 제형 후발의약품, 생물학적제제, 유전자재조합의약품, 세포배양의약품, 첨단바이오의약품 (의약외품) 신물질·신소재 사용 의약외품을 포함한 신규 허가 의약외품 (의료기기) 신개발·희소 의료기기를 포함한 신규 허가 의료기기 |
||
참고로 신약으로 당뇨환자의 혈당 조절 보조제 '마운자로프리필드펜주' 5개 함량을 지난달 28일에, 간세포암 치료제인 '이뮤도주(트레멜리무맙)'를 지난달 23일에 허가했으며, 희귀의약품으로 재발성 또는 불응성 미만성 거대 B세포 림프종 치료제인 '민쥬비주(타파시타맙)'를 지난달 9일 허가했다.
아울러 당뇨병 환자의 간질액 내 포도당 측정함으로써 혈당 수준을 연속적으로 모니터링하는데 사용하는 의료기기인 ‘개인용체내연속혈당측정시스템’의 국내 첫 제조 품목을 지난달 20일 허가했다.
식약처는 앞으로도 의료제품 허가 현황을 정례적으로 제공하겠다고 하였으며, 의료제품별 상세한 허가사항은 전자민원시스템에서 확인할 수 있다.
또한 식약처는 앞으로도 허가와 관련된 국민 관심이 높은 정보를 적극 발굴해 공개·제공하는데 최선을 다하겠다고 말했다.
의료기기뉴스라인
webmaster@kmdia.or.kr

