KMDIA BlueSky - 회원사를 위해 노력하는 협회


| ▶정책기획부 - 기획팀, 교육연구팀 |
■ [KMDIA] 의료기기 입문마스터 과정 4차 교육(10.04)
■ [보험위원회] 공급위기 대응 TF 회의(10.04, 11, 17, 24, 31)
■ [식약처] 의료기기 기준규격 개정 관련 의견 제출(10.04)
■ [심평원] 복강경, 흉강경, 관절경 치료재료 정액수가 개선 평가결과 안내(10.04)
○ 주요내용 : 3대경 치료재료 정액수가 비용을 5년간 단계적으로 행위수가로 전환
■ [식약처] 식품 의약품 분야 규제개선 과제 제출(10.05)
○ 주요내용 : 의료기기 허가정보공개범위 합리화 등 7개 사항
■ [식약처] 의료기기 규제개선 과제 제출(10.05)
○ 주요내용 : 의료기기 표준코드제도(영구표시대상) 개선 등 4개 사항
■ [법규위원회] 10월 운영진 회의(10.05)
○ 주요내용 : 협회 규제개선과제 제출현황 및 의료기기 심사자 제품 교육 공유
■ [심평원] 급여등재실 민원 업무협의 및 치료재료전문평가위원회 참석(10.05)
■ [심평원] 검강보험심사 업무 협의(10.06)
■ [법규위원회] 법규위-NIDS 심사자 제품 교육(10.06)
○ 주요내용 : 의료기기 제품 강연 및 실습
■ [건보공단] 빅데이터 정보 이용 관련 업계 의견제출(10.06)
○ 주요내용 : 빅데이터 정보 활용 업무의 산업계 불편사항 제출
■ [KMDIA] 의료기기 규제과학(RA) 전문가 2급 과정 4차 교육(10.07)
■ [국조실] 신의료기술평가 개선 관련 바이오헬스분과장 면담(10.07)
○ 주요내용 : 식약처 허가를 득한 의료기기의 허가 범위 사용의 신의료기술평가 개선 방안 논의
■ [식약평가원] 의료기기심사부 품목별 담당자 안내(10.11)
■ [KMDIA] 의료기기 수출 및 사후관리 과정(심화) 1차 교육(10.12)
■ [식약처] 첨부문서 내 부작용 정보 관련 사항 기재에 관한 업계 의견 제출(10.13)
■ [보험위원회] 10월 특별강연(10.13)
○ 주요내용 : 미국의 디지털헬스 건강보험정책 및 사례 소개
■ [보험위원회] 정액수가 치료재료 재평가 회의(10.14)
○ 주요내용 : 정액수가 치료재료 결과통보에 대한 이의신청 진행 여부 논의
■ [KMDIA] 의료기기 규제과학(RA) 전문가 2급 과정 4기 교육(10.14)
■ [식약평가원] `22년 하반기 체외진단의료기기 허가‧심사 2차 민원설명회(10.14)
○ 주요내용 : 코로나19 체외진단의료기기 신청문서(허가사항) 기재 표준양식 공유 및 최신 심사 기준 등 안내
■ [식약처] 의료기기 생물학적 안전성 평가자료 마련 협의체 회의(10.14)
○ 주요내용 : 의료기기 갱신관련 생물학적 안전성 평가자료 가이드라인 (안) 검토 및 의견 수렴 등
■ [복지부] 「요양급여대상‧비급여대상 여부 확인의 절차와 방법 등에 관한 기준」 등 2건 일부개정고시 안내(10.11)
○ 주요내용 : 디지털의료분야에 대한 요양급여대상‧비급여대상 여부 확인, 신의료기술 등 평가의 효율성‧전문성을 높이기 위해 디지털의료전문평가위원회 신설 근거 마련
■ [복지부] 「혁신의료기술의 평가와 실시 등에 관한 규정」 일부개정고시 안내(10.14)
○ 주요내용 : 혁신의료기술평가 절차 간소화 및 신속 평가
■ [체진협] 2022년 제4차 의료기기 ‘소유’ 회의 결과 안내(10.17)
■ [보험위원회] 공급위기 대응 TF 회의(10.17)
■ [NECA] 신의료기술평가 개선 간담회(10.19)
○ 주요내용 : 인체이식형의료기기가 아닌 중재적시술에 사용되는 의료기기의 신의료기술평가 유예대상 포함 건의
■ [식약처] 「혁신의료기기 지정 절차 및 방법 등에 관한 규정」 일부개정고시 및 관련 공고문 안내(10.19)
○ 주요내용 : 신속 제품화 지원을 위해 혁신의료기기 통합심사 등 식약처장과 복지부장관이 협의해 필요하다고 인정하는 경우 일정기간을 정해 지정 신청
■ [식약처] ‘혁신의료기기 지정 절차 및 방법, 기준 등에 관한 안내(민원인 안내서)’ 개정 안내(10.19)
○ 주요내용 : 혁신의료기기 통합심사 추가 및 일반심사(군별 지정기준) 개선 등
■ [식약처] 「추적관리대상 의료기기 기록과 자료 제출에 관한 규정」 일부개정고시 안내(10.19)
○ 주요내용 : 추적관리대상 의료기기에 대해 공급내역 보고를 한 경우, 추적관리대상 의료기기 유통기록을 제출한 것으로 간주
■ [보험위원회] 3대경 정액수가 치료재료 재평가 결과 이의신청서 검토(10.20)
■ [법규위원회] 법규위원회 관리분과 회의(10.20)
■ [KMDIA] 의료기기 품질경영시스템(ISO 13485:2016) 실습 과정 4차 교육(10.19, 20)
■ [보험위원회] 절삭기류 치료재료 재평가 방안 마련 연구용역 발주 회의(10.21)
○ 주요내용 : 2023년 예정된 절삭기류 치료재료 재평가 계획 관련 연구용역 발주
■ [보험위원회] Futures Club Junior 계획(안) 의견 수렴(10.21)
○ 주요내용 : 위원회 인재양성 프로그램인 Futures Club 1기 이후 좀 더 젊은 세대를 중심으로 활동할 수 있는 Futures Club Junior 프로그램 운영 계획(안) 마련 및 의견 요청
■ [심평원] 내시경하 시술용기구 재평가 간담회(10.26)
○ 주요내용 : 재분류 및 상한금액 조정(안) 관련 회원사 의견 제출 예정
■ [식약평가원] 의료기기 심사부 간담회 사전회의(10.26)
■ [식약평가원] 의료기기심사부 품목별 담당자(22.10.21) 안내(10.26)
■ [복지부] 치료재료 급여, 비급여 목록 및 급여상한금액표 일부개정고시 안내(10.26)
○ 주요내용 : 치료재료 중 본인일부부담 품목, 비급여 품목, 행위료 포함 품목, 100분의 100미만 본인일부부담 품목 신설 등(시행일 11.01)
■ [심평원] 급여등재실 업무 관련 개별 민원상담 수요조사(10.27)
○ 주요내용 : 11월 중순 급여등재실(등재관리부, 치료재료등재부, 치료재료평가부(TF), 의료기술등재부, 의료기술평가부) 업무 관련 업체 개별 애로 및 건의사항 해소를 위한 일대일 민원상담 추진 예정
■ [식약처] 의료기기 스타트업 지원 등을 위한 허가심사 회의(10.27)
○ 주요내용 : 허가/심사 효율화 방안 논의(제출자료 목록, 항목별 요건 적절성 여부 등 사전검토 방안)
■ [보험위원회] 10월 보험위원회 특별강연(2) 개최(10.27)
○ 주요내용 : 유럽의 디지털헬스 건강보험정책 및 사례 소개
■ [NIDS] 2022년도 의료기기 업계 간담회(10.28)
○ 주요내용 : 체외진단의료기기 허가 규정 해석, 부분품 추가 시 유의사항 안내 및 업계 의견 청취 등
■ [보험위원회] 복지부 보험정책국장 간담회(10.28)
■ [KMDIA] 의료기기 경영전략 수립 과정 2차 교육(10.28)
■ [보험위원회] 3대경 정액수가 치료재료 재평가 결과 이의신청서 제출(10.28)
○ 주요내용 : 환자 감염 및 예방이 시급한 품목에 한해 제한적으로 별도보상 건의 등
■ [보험위원회] 뇌혈관 수술 관련 급여기준 확대 의견제출(10.28)
○ 주요내용 : 기계적 혈전제거술용 치료재료 등 6개 품목 관련 의견
■ [NIDS] 1등급 의료기기 표준 신고 양식 마련을 위한 전문가 협의체 회의(2차)(10.31)
■ [보험위원회] 공급위기 대응 TF 회의(10.31)
■ [식약처] 의료기기 품질책임자 의무교육 이수 및 미이수에 따른 과태료/행정처분 안내(10.31)
○ 주요내용 : 의무교육 미이수에 따른 과태료 및 행정처분 2023년 예정
| ▶운영지원부 - 회계팀, 인사총무팀 |
■ [KMDIA] 협회 보안장비 펌웨어 업데이트 작업(10.04)
■ [KMDIA] 제4차 이사회 개최(22.10.12)
■ [KMDIA] 정규직 이세영 사원 임명장 수여식(10.17)
■ [KMDIA] 협회 제규정 업데이트(10.19)
■ [KMDIA] 대교육장‧대회의실 LED 스크린 설치(안) 보고(10.21)
■ [KMDIA] 2022년도 협회 워크숍(10.25)
| ▶대외협력부 - 홍보팀, 국제교류TF팀(IMDRF 지원사무국) |
■ [성균관대 삼성융합의과학원] 인재육성 협력 MOU 체결식(10.04)
○ 주요 내용 : 수요기반 인재육성을 통한 의료기기산업 분야의 발전을 위한, 포괄적 교육 협력 추진
■ [KMDIA] 제8회 자선골프대회 개최(10.05)
○ 주요내용 : 의료 소외계층 어르신, 아동의 건강한 사회 조성을 위한 기업의 나눔실천과 기부 문화 확산 마련
■ [복지부] 한-콜롬비아, 한-베트남, 한-캐나다 FTA 품목별 원산지 기준(PSR) 변환안에 대한 의견 수렴(10.05)
○ 주요 내용 : 국제표준 품목분류체계(HS코드) 변경에 따른 FTA 체결국 원산지 기준 개정 협상 관련 국내 수출업계 대상 의견조회 시행(~10.06(목))
■ [국회 보건복지위원회] 국정감사 모니터링(10.05~10.20)
■ [무역협회] EU 의료기기 시장진출 웨비나(10.06)
■ [인천테크노파크] 광역형 국산의료기기 교육훈련 지원사업 안내(10.06)
■ [한국무역협회] EU 의료기기 시장진출 웨비나 개최 안내(10.06)
■ [세비아코리아] 사무실 이전 기념식(10.07)
■ [KMDIA] 프레스 콘퍼런스 개최(10.07)
○ 주요내용 : 협회 최초 해외 전시플랫폼 개설 및 국산 의료기기 종합 전시회 베트남 론칭에 대한 홍보
■ [충북창조경제혁신센터] 2022 메드텍스쿨 하반기 교육 수강생 모집 안내(10.12)
○ 주요내용 : 의료기기 예비, 초기 창업자를 위한 사례 중심 교육
■ [KMDIA] 일본 도쿄 의료기기 전시회 한국관 참가(10.12~14)
○ 주요 내용 : 한국관 11개 업체, 12개 부스 운영
■ [진흥원] 테마가 있는 상담 사전 접수 안내(10.13)
○ 주요내용 : 의료기기의 신속한 해외 시장 진출을 위한 인허가 상담
■ [국제애드보커시] 2022 한국 의약품 및 진단기기 국제기구 조달과 국제 인증포럼 안내(10.17)
■ [한국인터넷진흥원] 2022 디지털 의료기기 보안시험·인증교육 안내(10.18)
■ [KMDIA] 2023 베트남 K 의료기기 전시회(K MED EXPO VIETNAM)」개최 및 참가업체 모집 안내(10.18)
■ [산업부] 2022 하반기 통상지원 통합 설명회(10.18)
○ 주요내용 : 해외진출‧관심 기업을 대상으로 급변하는 글로벌 통상이슈에 대한 진단 기회를 제공하고 기업 경쟁력 확보를 위한 통상지원정보 소개
■ [KOTRA] 2022년 중견기업 ESG+ 포럼 개최 안내(10.18)
○ 주요 내용 : ESG 도입을 통한 수출화대와 글로벌 가치사슬 편입 전략 모색
■ [KMDIA] 상생협력 TF 2차 회의(10.18)
○ 주요 내용 : 사업 구체화를 위한 데이터베이스(DB) 구축 방안 논의
■ [한국디지털융합진흥원] 바이오헬스 산업 활성화를 위한 AI 맞춤형 전문 교육생 3차 모집(10.19)
■ [IMDRF 지원사무국] IMDRF RPS 및 GRRP 자문 회의(10.20)
■ [분당서울대병원] 2022 엔데믹 시대, 의료기기산업의 개발 전략 포럼(10.24)
■ [KMDIA] 2022 남아공 요하네스버그 의료기기 전시회 한국관 참가(10.26~28)
○ 주요 내용 : 한국관 6개 업체 참가, 10개 부스 운영
■ [진흥원] 미 행정명령(14017)의 국내 의료기기 기업 영향 검토 업계 의견제출(10.26)
○ 주요내용 : 의료기기 포함 약 1,100여개 품목(초안) 발표(방역물품, 감염질환 진단 및 분석, 시약류 등)에 대한 업계 영향 제출
■ [국제교류위원회] ‘Medi-Talk: 일본 의료기기 시장 진출’ 웨비나 개최(10.27)
■ [국제교류위원회] ‘Medi-Talk: 일본 의료기기 시장 진출' 웨비나 만족도 조사(10.27)
■ [KMDIA] 임원사 GMS 윤정권 부사장 인터뷰(10.27)
■ [KMDIA] 부산 KIMES 2022 개막식 등 참석(10.28~10.30)
○ 주요내용 : 협회 홍보부스 운영 및 2023년 베트남의료기기전시회 개최
| ▶회원지원부 - 회원지원팀, 공정경쟁관리팀 |
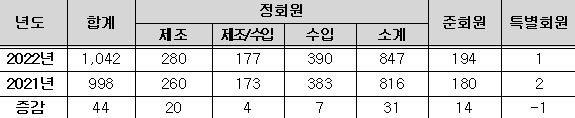
■ 회원사 현황
■ [KCL] 의료기기 전자민원창구 접수 및 GMP 등 교육(10.05)
○ 주요내용 : 의료기기 전자민원창구 접수 및 GMP 등 교육
■ [KMDIA] 의료기기 배상책임보험 관련 회의(10.5~7, 18, 26, 28)
■ [규약심의위원회] 제10차 공정경쟁규약 심의위원회(10.14)
○ 주요내용 : 기부, 학술대회 개최·운영지원, 학술대회 참가지원, 자사제품 설명회 및 교육훈련 심의, 사전·사후 신고사항 등 심의
■ [윤리위원회] 10월 전체 회의(온·오프라인)(10.19)
■ [유통구조위원회] 제19차 전체회의(온·오프라인)(10.19)
■ [KMDIA&KRPIA] 공동세미나 개최(10.21)
■ [특허청] 의료기기산업 특허유공자 표창 공적 심사(10.24)
■ [특허청] 의료기기산업 특허유공자 표창 후보자 상신(10.28)
| ▶공공사업부 - 통관관리팀, 광고관리팀 |
■ 표준통관예정보고 및 수입요건확인면제 업무처리 현황

■ [KMDIA] 제38~41차 자율심의기구 광고심의위원회(온오프라인 심의)(10.05, 12, 19, 26)
■ [KMDIA] 의료기기 광고심의 관련 민원상담(10.05)
○ 주요내용 : 이학진료용기구 광고의 사용 가능한 임상자료 활용 범위
■ [KMDIA] 의료기기광고 예비검토 기준 조정 회의(10.05, 12, 19, 26)
○ 주요내용 : 임상시험 결과의 광고 활용시, 실시기관 및 시험조건 등을 표시하도록 하되, 실시기관(의료기관)의 마크 활용 금지 등
■ [식약처] 22년도 의료기기 안전관리 유공자 포상 추천 상신(10.06)
○ 주요내용 : 통관관리팀 김민성 과장, 광고관리팀 이지연 대리 2인 추천
■ [관세청] 수리전반출 제도 개선 안내(10.06)
○ 주요내용 : 반도체장비, 의료기기 등 대형 시설장비에 대해 부분품별로 관세율을 적용하지 않고, 모든 부분품이 수입 완료될 때까지 완성품으로 수입신고 수리 및 완성품 관세율 적용
■ [KMDIA] 2022 일본 도쿄 의료기기 전시회 참관(10.12~15)
■ [식약처] 2022년도 3분기 의료기기 광고 모니터링 결과 제출(10.25)
■ [KMDIA] 의료기기 광고 자율심의 제도 인식 제고 홍보리플렛 발간(10.25)
| ▶산업연구부 - 미래전략연구팀, 정보분석팀 |
■ [혁신산업위원회] 홍보 및 소속 기업 소개자료 제작 배포(10.04)
■ [식약처] 공중보건 위기대응 의료기기 등 수급관리체계 구축 및 국산화 지원방안 마련 연구 1차 진도보고 개최(10.14)
○ 주요내용 : 연구 진도보고 및 주관부서 의견 청취 등
■ [진흥원] 보건산업진흥 보건의료 기술사업화 유공 포상 심사위원회(10.17)
■ [혁신산업위원회] 운영진 회의(10.18)
■ [혁신산업위원회] 특별강연(10.18)
○ 주요내용 : 혁신의료기기 관련 법/규정 개정사항, 디지털치료기기 건강보험 적용 관련 지불구조 동향 등
■ [식약처] 신기술 의료기기 안전규제 관리기준 마련 연구 전문가협의체 회의(10.26)
■ [식약처] 공중보건 위기대응 의료기기 등 수급관리체계 구축 및 국산화 지원방안 마련 연구 2차 진도보고(10.28)

