KMDIA BlueSky - 회원사를 위해 노력하는 협회


| ▶ 정책기획부 - 기획팀, 교육연구팀 |
■[보험위원회] 위원장 & 사무국 Weekly 회의(01.03, 10, 17, 24)
■[식약처] 의료기기 임상시험기관 지정현황 안내(01.03)
■[식약평가원] 2022년도 의료기기심사부 품목별 담당자 명단 공유(01.03)
■[정보원] 의료기기 통합정보 및 공급내역 보고 관련 가이드라인(2종) 개정 안내(01.04)
○ 주요내용 : 의료기기 표준코드(UDI) 및 공급내역 보고 제도 2종
■[심평원] 2022년 상반기 예비급여 추진항목 및 급여화 검토항목 자료 제출 안내(01.06)
○ 주요내용 : 연속혈당측정 내장형 인슐린 자동주입기, 휴대용 인슐린 자동주입기, 연속혈당측정용전극 3개 품목 급여화 검토 등
■[심평원] 신포괄지불제도 시범사업 지침 개정 안내(01.06)
○ 주요내용 : 포괄·비포괄영역구분 기준이 ‘1인당 사용금액, 사용분률·금액기준’으로 변경돼 약제 및 치료재료의 포괄·비포괄 영역 변경
■[심평원] 심원장 및 협회장 간담회(01.07)
○ 주요내용 : 코로나 19 상황 하의 산업계 지원 방안 논의
■[보험위원회] 신의료기술평가 개선 NECA 방문(01.07)
○ 주요내용 : 신의료기술평가에 관한 규칙 개정 진행사항 파악 및 의료기기 선진입 후평가를 위한 개선 방안 논의
■[IVD위원회] 3등급 IVD 재평가 임상적 성능시험 자료 관련 현황조사 결과 및 요건 수정(안) 검토 회의(01.10)
■[법규위원회] 식약처 GMP 심사 제도 운영 관련 간담회 결과 후속 설명회 (01.11)
■[식약처] 유럽 의료기기 규정(MDR) 시행 관련 업계 회의(01.12)
○ 주요내용 : MDR 전환에 따른 국내 제조업체 애로사항 청취 및 개선사항안 논의
■[심평원] 신포괄수가지불제도 지침 개정 회의(01.13)
○ 주요내용 : 신포괄지불제도 시범사업 지침 개정 관련 논의
■[보험위원회] 보험위원회 1월 특별강연(01.13)
○ 주요내용 : 심혈관 중재시술 로봇 개발 경험을 중심으로 의료로봇 실용화 고민
■[보험위원회] KMDIA 보험위원회 1월 특별강연(01.13)
○ 주요내용 : 심혈관 중재시술 로봇 개발 경험을 중심으로 의료로봇 실용화의 고민
■[식약처] 2022 의료기기 비임상시험실시기관 지정 현황 안내(01.13)
■[식약처] 의료기기 제조허가등 갱신에 관한 규정 일부개정고시 안내(01.14)
■[중소벤처기업진흥공단] 7차 규제자유특구 산업분야 전문가 1명 추천(01.14)
■[식약평가원] 의료기기심사부 품목별 담당자 안내(01.14)
■[IVD위원회] 3등급 IVD 재평가 임상적 성능시험 자료 관련 요건 개선(안) 및 업계 현황 제출(01.14)
■[식약처] 「의료기기 제조허가등 갱신에 관한 규정」 일부개정고시 안내(01.17)
○ 주요내용 : 이미 식약처장에게 보고한 의료기기 공급내역 보고자료에서 이전 유효기간 동안 생산·수입이 있음을 확인할 수 있는 경우, 해당 자료 제출 면제(2020.10.08 이전 기허가 및 재심사 의료기기에 대한 유효기간을 2025.01.01~2030.12.31 범위 지정)
■[식약처] 「의료기기법 시행령」 일부개정령 공포 안내(01.18)
○ 주요내용 : 무허가 등 위해 의료기기 제조·수입 시 해당 의료기기의 판매금액(판매가격*판매량)의 최대 2배 금액까지 징벌적 과징금 부과 등
■[식약처] 코로나19 변이 진단시약 관련 허가심사 설명회(01.18)
○ 주요내용 : 오미크론 등 변이 진단시약의 임상적 성능시험 기준 및 상세 시험법
■[식약처] 중국 도시 봉쇄에 따른 체외진단의료기기 원료 수급 동향 등 조사 안내 및 조사결과 회신(01.19)
■[복지부·심평원] 의료기기산업계 간담회(01.20)
○ 주요내용 : 획기적 가치평가 대상이 되기 위한 임상문헌 요건 완화 등
■[공정거래위원회] 시장진입 및 사업활동을 제한하는 법령, 제도에 대한 의견제출 요청(01.21)
■[보험위원회] 보험위원회 1월 특별강연(01.21)
○ 주요내용 : 신포괄수가지불제도 지침 개정이 치료재료에 미치는 영향 분석
■[식약처] 의료기기 생물학적 평가보고서 작성 가이드라인 마련 전문가 추천(01.21)
○ 주요내용 : 국내·외 위험관리 기반 의료기기 생물학적 평가 자료 수집 및 분석, 위험관리 기반 의료기기 생물학적 평가보고서 작성 가이드라인 마련 등을 위한 구성하는 협의체 전문가 추천
■[식약평가원] 코로나19 체외진단의료기기 허가심사 관련 안내(01.21)
○ 주요내용 : 변이 진단시약 허가·심사 신청 시 WHO 주요 변이(알파 등 5종)에 대해 제품성능에 미치는 영향을 평가한 자료 제출 등
■[IVD위원회] 3등급 IVD 재평가 임상적 성능시험 자료 회의(01.24)
○ 주요내용 : 재평가 임상적 성능시험 자료의 대체자료에 대한 예시 마련 및 검체 분양 기관 등 수급 기관 현황 파악 추진방안 등 논의
■[식약처] 「의료기기법 시행규칙」 일부개정령 공포 안내(01.24)
○ 주요내용 : 소프트웨어 의료기기 특성에 맞는 제조소 시설기준 등 마련
■[식약평가원] ‘의료기기의 사이버보안 허가·심사 가이드라인’ 개정 안내(01.24)
○ 주요내용 : IMDRF ‘의료기기 사이버보안 원칙 및 기준’의 적용범위, 정의, 시판 전 고려사항 적용
■[식약처] 소프트웨어 의료기기(SaMD) 사용적합성 관련 전문가 협의체 구성 산업계 전문가 3명 추천(01.24)
■[식약처] 의료기기 허가등 갱신의 안전성 평가자료 인정방안(비전기 분야) 관련 협의체 회의(01.25)
○ 주요내용 : 기허가 최초허가일 기준, 원재료 자사규격 변경 관련 이슈 등
■[법규위원회] 운영진 워크숍(01.26)
○ 주요내용 : 식약처 의료기기심사부 규제개선 간담회 추진 계획 등
■[IVD위원회] 허가심사분과 운영위원 회의(01.26)
○ 주요내용 : 체외진단기기과 간담회 안건 발굴 등
■[식약처] 의료기기 이상사례 표준코드 개정 관련 의견수렴(01.27)
■[복지부] 「신의료기술평가에 관한 규칙」 일부개정령 공포 안내(01.28)
○ 주요내용 : 의료현장에 선진입 가능한 의료기술 대상 및 기간 확대, 선진입 의료기술에 대한 안전관리 강화 등
| ▶ 운영지원부 - 회계팀, 인사총무팀 |
■[협회 필수교육] ROBOTIC SURGERY-미래컴퍼니(01.10)
■[현대회계법인] 2021년 회계 기말감사(01.14)
■[KMDIA] 2021년 귀속 내부감사(01.25)
○ 주요내용 : 협회 운영 전반 사항에 대한 자료요청 및 감사 진행
- 감사 수검에 따른 주요 지적사항 및 이슈 등 보고 (01.27)
| ▶ 대외협력부 - 홍보팀, 국제협력팀(IMDRF운영사무국) |
■[서울아산병원] 의료기기중개임상시험지원센터 기업지업프로그램 안내(01.03)
○ 주요내용 : 의료로봇, 의료 인공지능소프트웨어, 디지털 치료기기 등 실용화 추진 기업 지원
■[KMDIA] 국산 의료기기 사용 활성화 1차 회의(01.05)
○ 주요내용 : 실무추진협의회 운영 방안 논의
■[DITTA] 2022년 IMDRF-DITTA 합동 워크숍 준비 회의(01.06)
○ 주요내용 : 워크숍 주제 ‘의료용 소프트웨어 표준’
■[중앙보훈병원] 정형·재활 의료기기 사업화 인증 및 실증 지원사업 참여기업 모집 공고(01.06)
○ 주요내용 : 국내의 임상기술과 의료기기 사업화를 위한 정보제공, 임상검증 및 병원 연계 실증지원
■[KMDIA] 2022 터키 이스탄불 의료기기 전시회 한국관 참가업체 모집 안내(01.10)
■[진흥원] 2022 HIMSS USA 전시회 한국관 참여기관 모집 공고(01.11)
■[식약처] IMDRF 인공지능 의료기기 실무그룹 국제 회의(01.13)
■[KMDIA] 2022~23년 KOTRA 국고지원 단체참가 해외 전시회 선정 결과(01.15)
○ 주요내용 : 2022년도 일본 오사카(예비) 2022. 02. 24~02. 26 / 터키 이스탄불 2022. 03. 17~03. 19 / 필리핀 마닐라(예비) 2022. 08. 24~08. 26 / 남아공 요하네스버그 2022. 10. 26~10. 28 / 러시아 모스크바 2022. 12. 05~12. 09
■[YONSEI 혁신실증센터] 실증지원 및 시범보급 사업 홍보(01.17)
○ 주요내용 : 임상시험/비임상시험이 필요한 기업 실증지원
■[KMDIA] 의료기기협회보 신년호 제작 및 배포(01.17)
■[FICC(이스라엘상공회의소)] 이스라엘 업체 Business Offer 안내(01.18)
■[식약처] IMDRF 지원사무국 업무 추진 방향 및 운영 회의(01.18)
■[식약처] IMDRF 인공지능 의료기기 실무그룹 국제 회의(01.18, 20)
■[KMDICA] 국회 산업통상자원중소벤처기업위원회 업계 정책 간담회(01.18)
○ 주요내용 : 국내 의료기기 사용률 개선 위한 정책지원 필요
■[원주의료기기테크노밸리] 국내 기술문서 작성지원 모집 공고(01.18)
○ 주요내용 : 디지털헬스케어 산업 생태계 구축사업의 일환
■[산업부] 터키 임플란트 반덤핑 조사 최종보고서 관련 공청회 개최 안내(01.19)
■[KMDIA] KIMES 및 MEDICA 관련 업무 회의(01.20)
■[식약처] 2022년도 1차 의료기기 심사부 공무직근로자 채용 공고(01.20)
■[주한캐나다대사관] 한-캐나다 간 보건 의료산업 협업 회의(01.24)
■[KMDIA] 터키 이스탄불 의료기기 전시회 한국관 참가업체 모집 안내(01.24)
○ 주요내용 : 2022.03.17(목)~03.19(토) / 터키 이스탄불 Tüyap Fair & Congress Center
■[헬스경향] 언론인 미팅(01.25)
○ 주요내용 : 산업계 현안 공유 및 한국의약바이오기자협회 협업 등 논의
■[DITTA] 운영위원회 월례 회의(01.25)
○ 주요내용 : DITTA 실무그룹 활동 사항 업데이트
■[식약처] IMDRF 인공지능 의료기기 실무그룹 국제 회의(01.25, 27)
○ 주요내용 : AI 의료기기 가이드라인 초안 제출 전 최종 수정 작업
■[이씨플라자] 온라인 수출 플랫폼 구축 회의(01.25)
■[KMDIA] 언론기고 : 경향신문(협회장) 및 의학신문(법규위원회), 데일리메디(IVD위원회)(01.26)
■[복지부] 제10차 한-EU FTA 의약품, 의료기기 작업반 의제 발굴 요청(01.26)
■[KOTRA] 2022~2023년도 국고지원 해외 전시회 수행기관 선정 PT 심사(01.26)
○ 주요내용 : 2022-2023 미국 시카고 방사선 의료기기 전시회(RSNA) 수행기관 선정 PT
■[조달청] 2022년 해외조달시장 진출유망기업(G-PASS기업) 선정 공고(01.27)
○ 주요내용 : 상시 접수, 수출진흥협회(02-6203-7732), 조달청 조달수출지원팀(042-724-6443, 7590)
■[KMDIA] 2022 터키 이스탄불 의료기기 전시회 업무 회의(01.27)
○ 주요내용 : 한국관 위치 협의
■[포트리모트] 전시·박람회 협업 사업 미팅(01.28)
○ 주요내용 : 원격 박람회 플랫폼 소개 KIMES 참가 협회 회원사 대상 원격 상담 서비스 지원 논의 등
| ▶ 회원지원부 - 회원지원팀, 공정경쟁관리팀 |
■회원사 현황
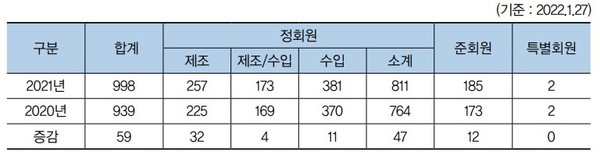
■[유통구조위원회] 제1차 임시회의(01.06)
■[유통구조위원회] 제2차 임시회의 개최(01.12)
■[규약심의위원회] 제1차 공정경쟁규약 심의위원회(01.14)
■[심평원] 간납사 실태조사 자문단 Kick-off 회의(01.14)
■[KMDIA] 제23회 한국의료기기산업협회 정기총회 유공자 포상 공적 심의(01.17)
■[규약심의위원회] 공정경쟁규약 및 세부운용기준 FAQ 개정사항 안내(01.17)
○ 주요내용 : 의료기기 거래에관한 공정경쟁규약 FAQ 및 체크리스트 법률검토 최종본
■[유통구조위원회] 2022년도 제10차 전체 회의(01.18)
■[심평원] 간납사 실태조사 1차 자문단 회의(01.20)
■[심평원] 간납사 실태조사를 위한 의료기기 유통 질서 자문위원 3명 추천(01.20)
■[규약심의위원회] 내부지침 의결사항 안내(01.21)
○ 주요내용 : 의료기기 거래에 관한 공정경쟁규약 세부운용기준 제7조(제품설명회) 제3항의 단서조항에 따라 제10조(자사제품설명회) 및 제11조(교육훈련) 관련 심의된 개최 계획의 단순변경은 심의 면제
■[규약심의위원회] 제12기 공정경쟁규약심의위원 명단 홈페이지 공지(01.22)
○ 주요내용 : 임기 2022.01.01~2022.12.31까지(1년)
■[식약처] 2022년 제15회 의료기기의 날 포상 대상자 추천&신청 안내(01.25)
■[유통구조위원회] 의료기기 유통 개선(안)을 위한 회원사 의견조회(01.26)
■[KMDIA] 제15회 의료기기의 날 행사장소 사전답사(01.28)
| ▶ 공공사업부 - 통관관리팀, 광고관리팀 |
■표준통관예정보고 및 수입요건확인면제 현황
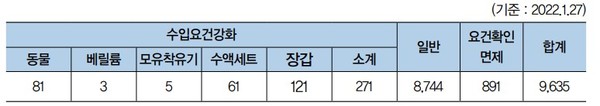
■[KMDIA] 제1차~제4차 광고심의위원회 심의(1.5, 12, 19, 26)
■[식약처] 의료기기 제조 반제품 업무 협의(01.18)
■[식약처] 협업검사 업무 협의(01.18)
■[식약처] 의료기기 광고 자율심의기구 간담회(01.20)
○ 주요내용 : 광고 자율심의기구 업무 애로사항 개선 방안 논의
■[식약처] 의료용 장갑 수입사항 업무 협의(01.27)
■[식약처] 의료기기 광고 자율심의 홍보영상 안내(01.28)
○ 주요내용 : 의료기기 광고 자율심의 제도 주요사항 알림
| ▶ 산업연구부 - 미래전략연구팀, 정보분석팀 |
■[KMDIA] 의료기기법 개정사항 발굴 회의 (01.06, 17, 24)
○ 주요내용 : 의료기기법 VS 약사법 비교분석 등
■[복지부 등] 2022년도 정부 R&D사업 온라인 부처합동 설명회(01.25~27)
○ 주요내용 : 22년 정부(과기부, 산업부, 중기부, 복지부, 질병청, 식약처) R&D 예산 주요 특징 설명

