■ FDA, 의료기기 세 분류로 허가 등록
■ 해외 의료기기 등록 규정 - 미국
미국, 세계 의료기기시장 44.9% 점유
FDA, 의료기기 세 분류로 허가 등록
미국 경제 동향
미국은 세계에서 4번째로 넓은 면적을 가진 나라이다. 면적은 한반도의 약 44.6배, 남한의 약 98.6배인 983.4만㎢에 달한다. 2017년 말 기준 미국 인구는 3.26억 명으로 중국(13.8억 명), 인도(12.8억 명)에 이어 인구 수 세계 3위를 차지하고 있다.

올해 미국 경제는 2017년보다 약 2.5%의 성장을 보일 것으로 예상된다. 국제경제 회복, 경제심리와 금융 시장 개선 등의 영향이 있을 것으로 예측하고 있다. 또 감세에 따른 가처분소득 증가 등으로 인한 소비지출 증가가 올해에도 이어지고, 달러 약세에 따른 기업 투자가 증가하는 현황이 미국 경제 성장에 긍정적인 영향을 끼칠 것으로 전망된다. 다만, 국제 무역규제의 변화와 트럼프 정부의 정치적, 경제적 불확실성이 존재하기에 한편으로 경제 성장을 제한할 여지도 있다.

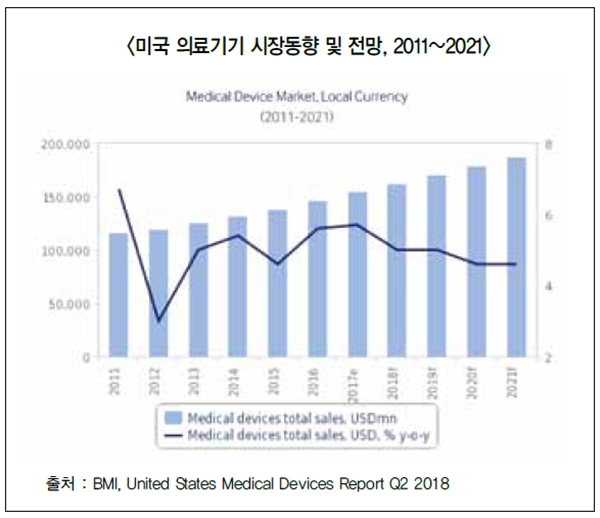
미국 의료기기 시장 동향 및 전망
미국 의료기기 시장은 2017년 기준 약 1,549.1억 달러 규모로 세계 의료기기 시장의 44.9%에 이르며 세계에서 가장 큰 시장이다. 2021년까지 미국 시장은 1,870.7억 달러로 성장할 것으로 전망되며, 2016~2021년 연평균 증가율(CAGR)은 달러 기준으로 5.0% 증가 할 것으로 예상된다. 또한 미국은 2016년 기준 GDP 대비 의료비 비중(17.6%)과 1인당 의료비 지출액(1만 203달러)이 모두 세계 1위를 기록하고 있다.
오바마케어가 2008년 시행된 이후 의료보험가입자 수가 증가하면서 전반적인 보건의료산업의 성장과 함께 의료기기 산업에 대한 관심과 수요도 더욱 증가했다. 이와 같은 추세로 인해 의료기기시장 규모는 더욱 확대될 것으로 분석된다.
반면, 자국의 제조 기술력이 높아 시장 내 수입 제품에 대한 비중이 낮은점과 복잡하고 까다로운 규제 그리고 제조시설의 운영비용이 높은점은 미국 의료기기시장 성장의 저해요인이기도 하다.
인구 측면을 살펴볼 때, 미국은 인구의 1/4이 베이비붐 세대(1946~1964년 사이 출생)이며 이들의 노령화로 인해 고령인구가 급증할 것으로 예상된다. 65세 이상 인구는 2017년 기준 5,105.5만 명으로 총인구의 15.6%를 차지하며 2030년 19%, 2040년에는 초고령사회에 진입할 것으로 예상된 다. 즉, 고령인구 증가에 따른 만성질환 증가 등으로 의료기기 수요는 앞으로 더욱 증가할 전망이다.
또한, 의료인프라 역시 세계 최고 수준을 유지하고 있다. 미국 내 전체 병원의 수는 2016년 기준 5,540개이며 병원 내 최신 의료장비 구비율도 최고 수준이다. 이중 민영병원은 4,362개로 전체 병원의 78.7%로 높은 비중을 차지하고 있다.
미국 의료기기 수출입 현황
미국은 세계에서 가장 큰 의료기기 소비처이면서 세계 1위의 수출국으로 해마다 작게나마 수출 규모를 늘려가고 있다. 2011~2016년 기준 연평균 (CAGR) 1.7%씩 증가했으나 2016년에는 전년대비 0.2% 감소해 442.2억 달러를 기록했다.
이 중 규모가 가장 큰 수출국은 네덜란드이다. 미국 전체 의료기기 수출의 11.7%인 51.8억 달러를 수출했다. 그 다음은 일본(46.0억 달러, 10.4%), 벨기에(40.3억 달러, 9.1%), 중국(37.9 억 달러, 8.6%), 캐나다(35.1억 달러, 7.9%) 순으로 나타났다. 한국은 8.3억 달러로 14위를 기록했으며 수출 비중은 1.9%이다. 주요 수출 품목은 의료용 소모품 (20.9%), 진단용 영상기기(20.4%), 정형용품(14.4%), 환자보조용 기기(8.7%), 치과용품(3.4%) 순이다.
미국 의료기기 시장에서 외국산 의료기기 비중은 약 30%를 차지한다. 수입 의료기기는 2016년 기준 전년대비 6% 성장률을 보이며 439.4억 달러를 기록했다. 국제금융위기가 한창이던 2009년엔 5.9% 하락세를 보인 경우를 제외하고 미국의 의료기기 수입 규모는 지난 10년간 꾸준한 성장세를 보여왔다. 수입 규모는 2011~2016년 기준 연평균(CAGR) 4.5% 증가했으며, 높은 제조시설 운영 부담으로 멕시코와 아일랜드와 같은 외국으로 제조시설을 이전한 영향이 미쳐 성장세가 이뤄진 것으로 분석된다.
이에 따라 멕시코에서 가장 많은 의료기기를 수입하며 금액은 75.9억 달러(17.3%)를 기록했다. 그다음이 아일랜드(57.3억 달러, 13%), 독일(52.8억 달러, 12%), 중국(50.9억 달러, 11.6%), 스위스(25.5억 달러, 5.8%) 순으로 수입액 규모를 보였다.
한국은 18위로 1.2%를 차지하는 5.13 억 달러를 기록하고 있다. 주요 수입 품목은 진단용 영상기기(20.8%), 의료용 소모품(17.8%), 정형용품(16.1%), 환자보조용 기기 (13.8%), 치과용품(4.8%) 순이다.


한국(대 미국) 의료기기 수출입 현황
미국은 2016년 기준으로 한국에 14.7억 달러(전년대비 7.25% 증가)의 의료기기를 수출했으며, 이는 한국의 전체 의료기기 수입액(31.5억 달러)의 46.8%를 차지한다. 또한 최근 식품의약품안전처의 ‘2017년도 의료기기 실적보고’보도자료에 따르면, 지난해 한국은 미국산 의료기기를 16.4억 달러 수입했으며 이는 전체 수입액(35.0 억 달러)의 46.95%를 차지하며 전년 대비 수입액과 비중이 함께 증가했다.
2016년도 주요 수입 품목은 소프트콘택트렌즈(1억 2,619만 달러), 스텐트(9,074만 달러), 인공무릎관절 (5,652만 달러), 혈관내튜브·카테터(5,160만 달러), 전기수술기용전극(4,652만 달러)로 나타났다.
또한 한국이 가장 많은 의료기기를 수출하는 나라가 미국이다. 2016년도 약 5억 달러(전년대비 4.46% 증가)를 수출했으며, 국내 의료기기 총 수출액(29.2억 달러)의 17.2%를 차지한다. 지난해에는 5.1억 달러를 수출했으며 전년대비 2.14% 증가한 규모로, 한국 의료기기 총 수출액(31.6억 달러)의 16.2%를 점유하여 1위를 유지했다.
2016년 대비 2017년 한국 대 미국 의료기기 수출 규모는 2.14%의 성장률을 나타냈다. 2016년도 주요 수출 품목은 의료용 프로브(1억 491만 달러), 초음파영상 진단장치(7,074만 달러), 의료용영상 처리용장치·소프트웨어(5,430만 달러), 면역화학검사지(3,002만 달러), 디지털엑스선촬영장치(2,893만 달러) 순이다.


미국 의료기기 규제기관 및 규제
미국은 의료기기를 보건복지부(Department of Health and Human Services, HHS)에서 종합적으로 관리·감독한다. 의료기기 심사는 보건 복지부 산하기관인 식품의약품안전국 (Food and Drug Administration, FDA)에서 담당하며 미국에서 의료기기를 판매하기 위해서는 FDA의 승인을 받아야 한다. FDA는 식품, 의약품, 화장품, 의료기기 등에 대한 사전검사 및 승인, 사후검사를 통한 부적합 제품의 제재 그리고 수입품과 일부 수출품의 효능과 안전성을 관리하는 역할을 수행한다.
미국의 의료기기에 관한 기본법은 FD&C 법이며, 해당법을 시행하기 위한 세부규정으로 CFR(Code of Federal Regulations)이 있다. 즉, FDA가 의료기기 허가, 관리 등 각 기기별 등급과 미국 내 시판을 위해 국내 외 제조업자가 취해야 할 절차 및 의무를 규정하고 있다. 이와 함께 FDA에서는 CFR에서 규정하지 못한 내용을 수십 개의 지침(Guidance)에 담아 시행하고 있다.
미국 의료기기 분류 및 등록 절차
미국은 의료기기의 정의를 FD&C 법(Federal Food Drug & Cosmetic) 의 Section 201(h)에서 위와 같이 규정하고 있다. 의료기기는 용도, 복잡성 그리고 위험도 등에 따라 3등급으로 분류되며 각 등급별로 요구하는 서류와 심사절차가 달라진다. Class I에는 저위험도, Class II는 중위험도, Class III는 고위험도의 의료기기가 각각 분류돼 있다. 각 의료기기별 등급은 21 CFR Parts 862~892에서 규정하고 있다.
각 의료기기의 등급은 FDA 홈페이지의 ‘Product Classification’에 의료기기의 정보를 입력하면 확인할 수 있다.
(https://www.accessdata.fda. gov/scripts/cdrh/cfdocs/cfpcd/ classification.cfm)
의료기기 등록 절차는 의료기기의 등급에 따라 3가지로 분류한다. 이 분류에 따라 FDA 510(k)(시판 전 신고) 또는 PMA(시판 전 승인)를 받아야 한다. 인증별 제출 서류와 절차가 다르며 소요되는 기간은 평균 약 7.2개월이나 경우에 따라 차이가 있다.
1등급 의료기기는 최소한의 규제를 받는 제품으로서 ‘일반규제’를 준수해야 한다. 일반규제사항으로는 △21CFR 807.2 항의 등록이 필요한 회사의 시설 등록(FDA 양식 2981 사용) △FDA에 출시될 의료기기 리스트 제출(FDA 양식 2892 사용) △21CFR 820조의 품질시스템규정(GMP)에 맞는 의료기기 제작 △21CFR801조 또는 809조의 표시기재 사항에 맞는 의료기기의 표시 기재 △의료기기의 출시 전 시판 전 신고서 510(k)의 제출이 있다. (의료기기의 출시 전 시판 전 신고서 510(k)의 제출은 1~3등급의 모든 의료기기에 적용된다.)
2등급 의료기기는 ‘일반규제’를 준수함과 동시에 ‘특별규제’를 준수해야 한다. 특별규제사항에는 특별표시기재사항 요건, 강제적 또는 자발적인 성능기준과 시판 후 감시를 포함한다.
대부분의 3등급 의료기기는 ‘일반규제’와 ‘특별규제’를 준수하는 사항에 추가적으로 ‘시판 전 허가(Premarket Approval, PMA)’가 요구된다. PMA는 3등급 의료기기의 안정성과 효능 을 확인하기 위한 과학적 심사과정으로 시판 전 심사의 가장 엄격한 절차이다.
PMA 심사과정은 서류심사와 제조시설 및 임상시험 실시기관에 대한 직접 방문을 통한 심사를 포함해 의료기기에 대한 안전성 및 유효성, 제조시설에 대한 확인, 임상시험 실시에 대한 적합성 등에 대한 확인절차를 거치게 된다. 등록하고자 하는 3등급 의료기기의 PMA 대상 여부는 FDA 홈페이지의 ‘품목분류 데이터베이스(Product Classification Database)’에서 확인 가능하다.
| 출처 1. BMI, United States Medical Devices Report Q2 2018 (2018.03) 2. FDA, www.fda.gov 3. CIA, The World Factbook (2018.04) 4. KOTRA, Global Market Report ‘한눈에 보는 수출유망국(의료기기 2편)’ (2017.12.22.) 5. KOTRA, 국가정보-미국 6. 식약처, 2016년도 실적보고 통계자료 7. 식약처, 2017년도 실적보고 보도자료 8. 보건산업진흥원, 보건산업브리프 의료기기해 외시장분석 vol.41 (2016.6.21.) |

