진흥원, 지난 2일부터 내달 10일까지 신청기간
[한국보건산업진흥원 공고 제2017-1호]
국산의료기기 신제품 사용자(의료기관) 테스트 지원사업 공고
2017년도 ‘국산의료기기 신제품 사용자(의료기관) 테스트 지원 사업’을 수행할 기관을 다음과 같이 공모하오니 관련 의료기관 및 기업체의 적극적인 참여를 바랍니다.
한국보건산업진흥원장
1. 사업 개요
□ 국산 신제품의 브랜드 인지도와 신뢰성 확보를 위해 사용자(의료기관) 테스트 지원
○ 수입 제품 위주로 사용 중인 국내 주요 의료기관을 통해 국산화가 가능한 유망 신제품의 테스트 및 시장진입을 지원
- 의료기관 사용자의 테스트를 통한 국산 신제품의 우수성 검증 및 성능 개선
○ 브랜드 파워가 있는 의료기관의 테스트 결과를 적극 홍보하여, 중소 의료기기기업 제품의 대학병원 진출, 수출 확대, 브랜드 인지도 강화를 통한 시장진출 지원
※ 테스트 예시
① 국산 신제품과 병원에서 기존에 사용하던 제품(외산)과의 비교 테스트
② 국산 신제품의 임상효능 검증 및 성능개선을 위한 테스트 등
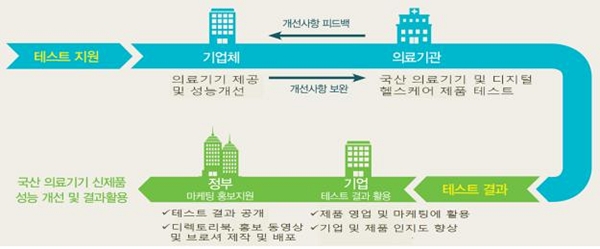
<국산의료기기 신제품 사용자(의료기관) 테스트 지원 체계>
□ 사업기간 : 2017년 3월 ~ 11월 (9개월)
※ 단년도 사업의 테스트 기간은 9개월 이내에서 자율 신청 가능하며, 제품의 특성 및 테스트 방법에 따라 다년도 사업으로 ‘18년 6월까지 신청 가능(사업 신청 시 기재)
2. 사업 내용
□ 지원 대상
○ (지원기관) 주관기관(의료기관)과 참여기업(제조기업)으로 구성된 컨소시엄
- 주관기관 : 상급종합병원(의료법 제3조의4) 또는 대학병원(치과대학·한의과대학 포함)
- 참여기업 : 테스트 대상 제품을 제조한 국내 제조기업(중소기업 등)
○ (지원 제품) 식약처 의료기기 제조 허가·인증 및 신고 후 시장 진입을 준비 중이거나 판매 초기인 국산 신제품*
- 테스트 제품이 대학병원 등 종합병원(치과병원·한의과병원 포함)에서 교체·구매 가능한 품목으로 선정
* 의료기기법 제2조 제1항(정의)에 해당되는 제품으로, 대학병원 등 종합병원(치과병원·한의과병원 포함)급 시장 진입하여 국산 점유율 상승이 가능한 제품
- 주관기관은 다수의 제품을 테스트할 경우, 별도의 컨소시엄을 구성하여 신청
※ 주관기관은 동일 제품의 테스트를 위해 2개 이상의 세부과제(타 진료과 및 의료기관 등) 구성 가능
- 참여기업은 자사 제품 2개까지 신청 가능(별도 컨소시엄 구성)
□ 지원 내용
○ 정부는 주관기관이 국산 신제품 테스트에 필요한 소요비용(과제당 최대 5,000만원/연 이내) 지원
- 테스트 인력 인건비, 재료비, 시험비, 의학회 홍보비(학술발표) 등
※ 정부지원 금액은 최종 선정된 과제 수, 과제 규모 등을 검토하여 조정 될 수 있음
※ ‘18년도까지 테스트 수행 컨소시엄은 전체의 30% 이내로 선정 예정
□ 지원 조건
○ (주관기관) 국산의료기기 등 신제품 테스트에 필요한 인력 및 공간, 시설 등을 제공
○ (참여기업) 전체 테스트 비용의 50% 이상을 부담
- 정부지원금의 최소 30% 이상은 기업부담금(현금)으로 부담하고, 테스트에 필요한 자사·경쟁사·소모성 제품 등은 반드시 현물로 부담
※ (예시) 정부지원금 50백만원 신청 시, 기업부담금(현금) 15백만원 이상 + 현물 35백만원 대응(참여기업 인건비 편성 불가)
□ 주요 사업내용
○ 테스트 제품 평가(주관기관)
- 주관기관은 사업기간동안 테스트 제품을 사용하고, 제품의 성능을 평가
※ 제품 우수성 입증, 성능 개선 등 명확한 목적을 설정하여 사업종료 후 마케팅, 성능개선 등에 활용될 수 있도록 테스트 계획 수립 및 사업수행
○ 테스트 제품 개선(참여기업)
- 주관기관의 연구책임자는 테스트 제품을 사용한 의견을 참여기업에 피드백
- 참여기업은 주관기관의 제품 사용 의견을 토대로 테스트 제품의 개선사항 발생 시 성능을 지속적으로 개선
○ 테스트 성공 제품의 결과 활용(주관기관-참여기업)
- 주관기관은 테스트를 통해 입증된 제품 우수성을 논문 게재, 의학회 발표 등 성과물 창출
- 정부는 테스트 결과를 공개, 참여기업은 테스트 결과를 마케팅*에 활용
* 테스트결과 홍보라벨 활용가능 (품목명, 기업명, 제품명, 테스트병원, 테스트책임자, ‘테스트 완료’ 등을 표시, 복지부, 진흥원, 테스트병원 로고 포함) : 라벨샘플 추후 제작 및 배포 예정
| 구분 | 사업내용 | 사업목표 |
| 1 | 테스트 제품 평가 | 평가 보고서(성능, 사용편의성 등) 제출 |
| 2 | 테스트 제품 개선 | 제품 테스트 후 개선의견 제출 * 의료기기의 경우, 변경된 기술문서 또는 식품의약품안전처 변경 허가서 추후 제출 |
| 3 | 테스트 결과 활용 | 테스트 결과에 대한 논문 등 학술대회 발표 및 매출액 추이 제출 * 논문의 경우 게재예정증명서 인정 * 사업 종료 후, 3년 이내까지 해당 제품 논문 및 매출 실적 조사 (의료기관 진입 여부 포함) 예정 |
3. 신청기간 및 방법
□ 공고 및 신청기간
○ 1.2 ~ 2.10 (6주간)
□ 신청방법
○ 우편 및 방문접수
- (28159) 충청북도 청주시 흥덕구 오송읍 오송생명2로 187 오송보건의료행정타운 한국보건산업진흥원 5층 의료기기산업지원팀
- 2.10(금) 18:00 限 도착분에 한함
□ 신청서류
○ 사업신청서(별지 서식) 10부 (전자문서는 e-mail, USB, CD 등의 방법으로 별도 제출)
※ 한국보건산업진흥원 홈페이지(www.khidi.or.kr) 사업공고 등에서 다운로드
○ 공통 구비서류 : 주관기관 및 참여기업 법인등기부등본(또는 사업자등록증) 1부
※ 접수된 자료는 반환하지 않음
□ 문의처
○ 한국보건산업진흥원 의료기기산업지원팀 채희석 연구원
(043-713-8147, E-Mail : hschae80@khidi.or.kr)

