상단영역
UPDATED : 2024-04-24 17:41 (수)
제보
실시간뉴스
본문영역
식약처 목록 ( 총 : 223건)
기사목록 보기 형태
-

-
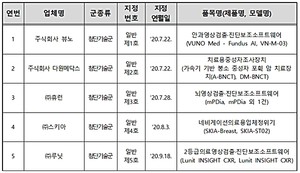
-

-

-
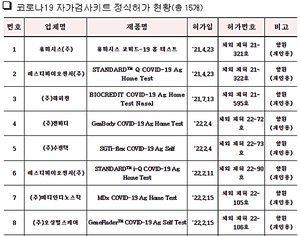
-
혁신 의료기기 지정 공고(일반 제30호)
「의료기기산업 육성 및 혁신 의료기기 지원법」제21조 및 같은 법 시행령 제15조에 따라 혁신 의료기기로 지정되어 붙임과 같이 공고합니다.< 혁신 의료기기 지정 공고 내용 >
-
23-3차 혁신의료기기 지정 통합심사 신청 공고
-
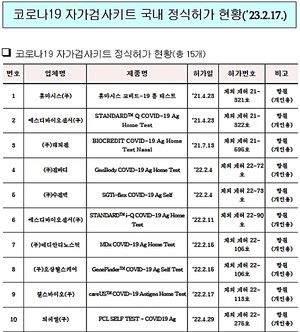
-
혁신의료기기 지정 공고(통합 제29호)
-

-

-
식약처 코로나19-독감 체외진단의료기기 민원설명회 자료 공개 알림
-
체외진단의료기기 임상적 성능시험 점검 계획
-
일회용발조절식전기수술기용전극 관련 의료기기 안전성 정보 알림
-
임상적 성능기험 종사자 교육 실시기관 변경사항 알림
-

-

-

-
혁신의료기기 지정 통합심사 신청 공고(제2023-046호)
-

